March 28, 2019
Elizabeth Denton
アミノ酸側鎖の様々な官能基は、二次構造と相まって、ペプチドやタンパク質に独自の特性と活性を与えています。しかし、ペプチドや小さなタンパク質を化学的に合成する場合、側鎖の官能基は合成を困難な方向に向かわせることがあります。
この投稿では、メチオニンを含むペプチドの合成と、このアミノ酸に関わる重大な副反応を克服する方法について説明します。
メチオニンとシステインは、天然に存在する20種類のアミノ酸の中で、側鎖に硫黄原子を含むたった2つのアミノ酸であり、その硫黄原子が独特な反応性プロファイルをもたらします。システインは、共有結合で二次構造を安定化させるジスルフィド結合を形成する特性でよく知られています。しかし、合成の観点からは、システインのチオール基は(しばしばトリチル保護基で)保護されており、合成中の望ましくない副反応に対してほとんど防ぐことができています。
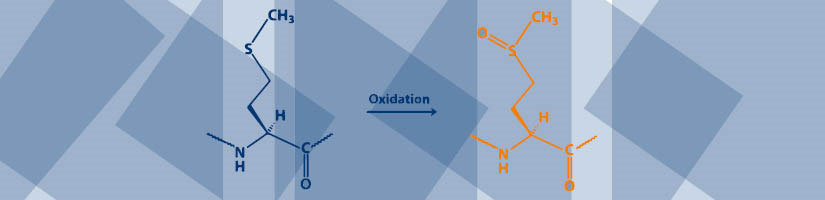
しかし、メチオニンは、末端がチオエーテル側鎖になっており、様々な活性酸素種によって非常に酸化されやすいため、酸化ストレスのマーカーとして最も注目されています。メチオニンのチオエーテルは、標準的なFmocベースの固相ペプチド合成では非反応性であることが分かっており、したがって保護されることはほとんどありません。しかし、残念ながら、このチオエーテルは、合成時および樹脂からの切り出しの両方において、酸化に対して敏感になります。
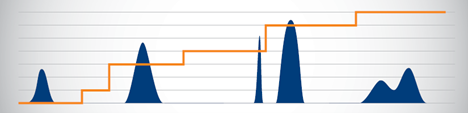
アミロイドβペプチド(残基1-42)の合成の最適化を行っており、ある実験を行うことにしました。これまでメチオニンを含むペプチドをほとんど扱ったことがなかったため、メチオニンの酸化がどの程度起こるのか興味がありました。アミロイドβは、合成が難しいペプチドとして知られているだけでなく、C末端から8残基目にもメチオニン残基を含んでいます。私は、合成中にアミノ酸溶液とリアクターバイアルを不活性雰囲気にはしない環境を構築し、Reagent Bカクテルから一部のスカベンジャーを除いたTFAカクテル(95:2.5:2.5 = TFA:水:TIS)を使って、樹脂からペプチドを切り出しました。この条件下での合成では、酸化メチオニンが多く生成したこと(目的分子量に対して16 Daの質量増加で示される)を確認しました(図1)。
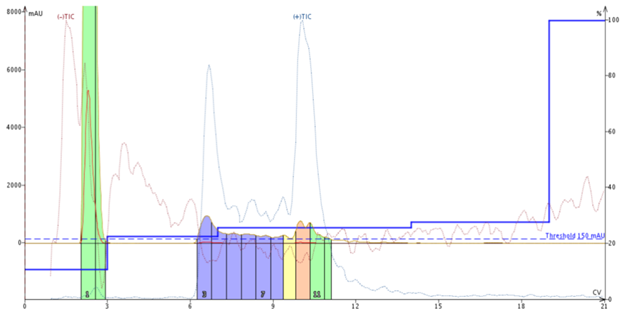
図1:アミロイドβ(1-42)の粗サンプル分析結果。メチオニンの酸化防止策を講じない場合、溶液中には約50:50で目的生成物:酸化メチオニンが含まれていました。
メチオニンの酸化を抑える、あるいは除去する確立された方法がいくつかありますが、今回の合成ではそのすべてを実施しませんでした。では、どのように対処するのが良いでしょうか? 生物学では、この反応を逆転させる方法が明確に発見されていますが、化学的プロセスでも適用できるものはあるのでしょうか?
メチオニンの酸化は主に樹脂からのTFAによる切り出し時に発生することから、90年代後半にHuangとRabensteinは新たな切り出しカクテルを開発しました。彼らは、ジメチルスルフィドとヨウ化アンモニウムを加えることで、ペプチドの収率を大きく損なうことなく、酸化メチオニンの存在を著しく低減または排除できることを見出しました。
これらと同様の試薬は、必要に応じて溶液中の酸化メチオニンを還元するために使用されています。C末端のチオエステルを維持したまま、ネイティブケミカルライゲーションでライゲーションするフラグメントペプチドの合成において、この試薬のオプションは非常に重要になります。
ペプチド合成に対して化学的なステップをいくつか追加しなければなりませんが、ペプチド全体を再合成することなく、この副反応を解決する方法があることを知って、少しほっとしました。
ジスルフィド結合の形成のように、酸化が良い結果をもたらす場合もあります。樹脂のジスルフィド結合形成の自動化については、下記Webinarをご覧ください。Webinarのプレゼンテーション資料もダウンロード可能です。
Webinar: Synthesizing Disulfide-rich Peptides
https://www.biotage.com/blog/webinar-synthesizing-disulfide-rich-peptides
参考資料:
酸化に対して敏感: Methionine sulfoxide- and sulfone-containing peptide synthesis: management of a relevant post-translational modification in proteins (Oligos & Peptides, 33(2), 2015, P32-36)
HuangとRabensteinは新たな切り出しカクテルを開発:A cleavage cocktail for methionine-containing peptides (The Journal of Peptide Research, 53, 5, 1999, 548-553)
溶液中の酸化メチオニンを還元:The reduction of oxidized methionine residues in peptidethioesters with NH4I–Me2S (Organic & Biomolecular Chemistry, 4, 2006, 2291-2295)
ネイティブケミカルライゲーション:Synthesis of Native Proteins by Chemical Ligation (Annual Review of Biochemistry, 69, 2000, 923-960)
元の記事:How to handle peptides that contain methionine? (biotage.com)
日本語化:2024年10月
PDFファイルダウンロード(277KB)