July 27, 2020
Elizabeth Denton
疎水性ペプチドの取り扱いに関しては日々議論されていますが、親水性ペプチドの精製に関してはそれ自体が課題となっています。以前の投稿で、私は極めて親水性の高いペプチドである アルギニンが8個繋がったOcta-Argを合成しました。このペプチドを精製する際にはイオン対試薬を使用して、カラムでの全体的な保持量を増加させました。しかし、フラッシュカラムクロマトグラフィーによる精製のためにどのような溶媒でペプチドを溶解させるかについては簡単なことではありませんでした。
本日の投稿では、精製時におけるペプチドサンプルのチャージで一般的に使用される溶媒について検討し、カラムのメディアによるペプチドの保持に対する影響について評価したいと思います。
HPLCを用いたOcta-Argの分析において、このペプチドはC18カラムに保持されていないことが明らかになりました。幸いなことに、この時実施していた検討は完了することができていました。しかし、この経験は、高純度のペプチドを得るためには注意する必要があることを示しました。
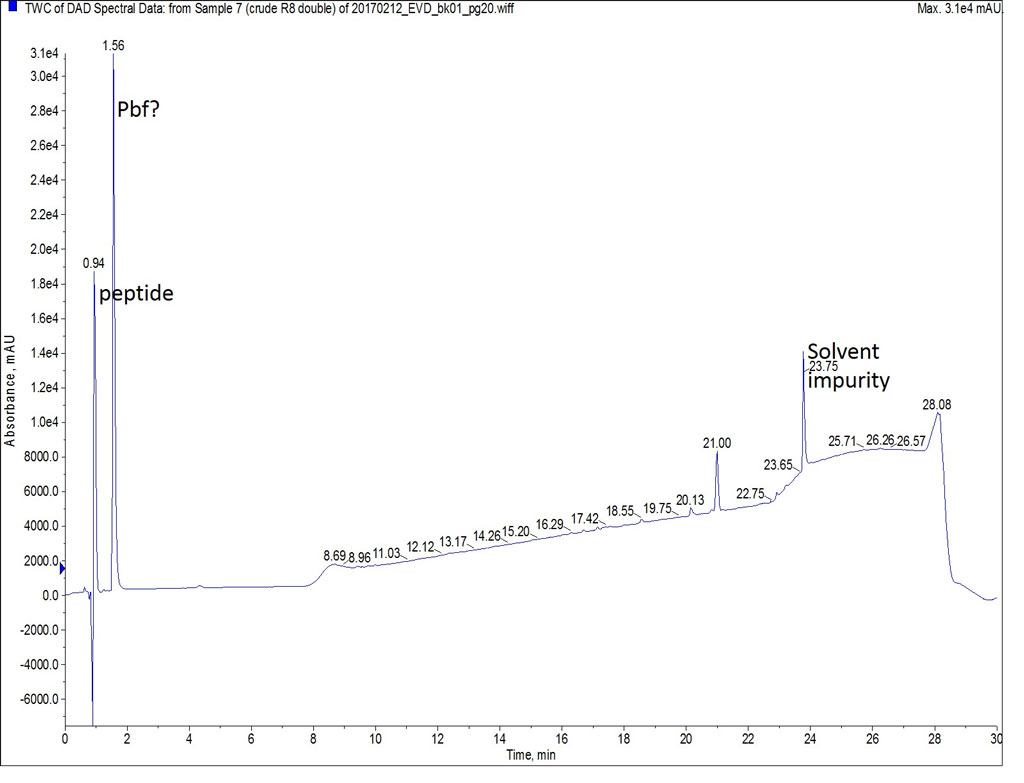
図 1: メタノールに溶解した粗Octa-Argの分析用HPLCの結果を示します。このペプチドはC18では保持されませんでした。
精私はペプチドケミストとして、ペプチドを溶解する溶媒が精製にどのような影響を与えるか についてあまり 考えていませんでした。しかし、このペプチドについては、精製を成功させるために溶媒強度を考慮しなければなりませんでした。私の同僚である ボブ・ビックラー は、様々な溶媒で低分子化合物を溶解しながら多くの逆相精製を行って研究を進めてきたので、Octa-Arg を精製するために これらの条件を応用して検証を行いました。
最初の実験ではあまり良い結果ではありませんでしたが、まずはメタノールから評価を始めることにしました。フラッシュクロマトグラフィーによる精製では、最少量の溶媒(Link)で最大量のペプチドを溶解することが目標であることを忘れないでください。Octa-Arg はメタノールには極めて溶けにくかったです(図2)。

図 2: Octa-Argをメタノールでの溶解を試みました。30mgの粗ペプチドを1mLのメタノールを添加しましたが、十分に溶解しませんでした。
このペプチドで溶解性の問題があったため、私はこの条件での精製を追求しませんでした。どのようなクロマトグラフィーにおいても、サンプル中に不溶性の沈殿物を伴う溶媒でのインジェクションは最終的に良い精製帰にならないと考えるからです。
そこで私は方針を転換することにしました(図3)。ペプチド合成において通常使用されている DMF を試してみようと思いました。チャージの溶媒として良く使用されている DMSO では一部のアミノ酸で起こる酸化の懸念がなく、DMF は高極性であり、ペプチドサンプルを高濃度で溶解できると考えました。

図 3: 精製用DMFに溶解したOcta-Arg 30mgの粗ペプチドを1mLのDMFに溶解しようと試みました。
このペプチドはメタノールよりも DMF に可溶であると思われましたが、この条件では完全にペプチドを溶解することができず、依然として精製には適していないことがわかりました。極性溶剤を大きな容量でチャージする場合は、溶液中に存在する沈殿物に由来する懸念に加えて、小さな C18 カートリッジを用いる精製に 悪影響を与える恐れがあります。現時点では、この条件で精製を進めないことにしました。
これまでの結果から溶媒として DMSO に頼りました。私の経験から、ペプチド100mgに対して100uLで溶解できることが多いので、ペプチドを溶解するために DMSO を頻繁に使用しています。チャージ量を一定に保つために、私は Octa-Arg 30mgを DMSO1mLに溶解しました。ペプチドは最終的に完全に溶解されましたので、私はこの条件で精製を実施しました(図4)。
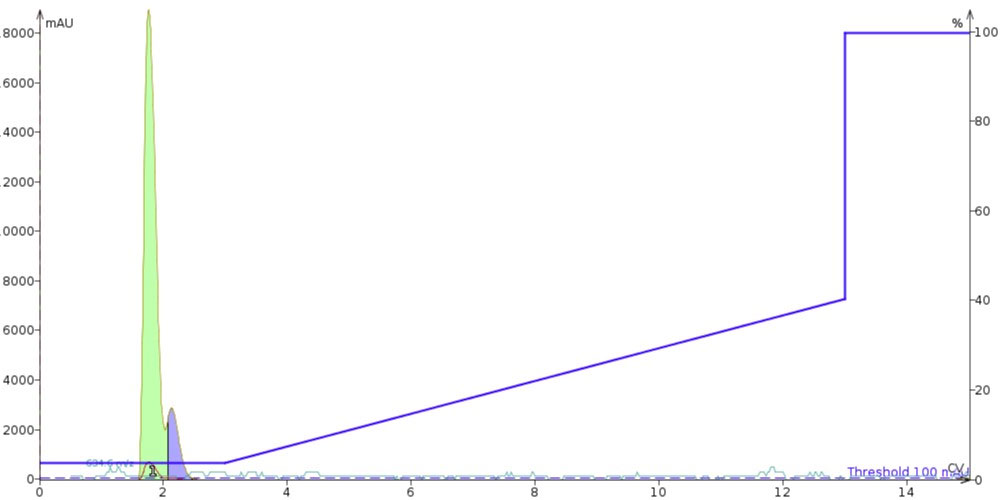
図 4: Octa‐Arg を DMSO に溶解し、10CV 以上でアセトニトリルの濃度を 3% から 40% のグラジエントを用いて精製を行いました。
DMSO の極性と溶媒強度は、この極めて親水性の高い Octa-Arg ペプチドの固定相アルキル鎖による保持するために必要な移動速度を明らかに制限しています。精製では高いサンプルの濃度が望まれますが、ペプチドが固定相によって保持され得ない場合、サンプルが目的の精製を達成する可能性は極めて低くなります。
最後の手段として、私は酸性の水にペプチドを溶解することにしました。これは、最初の移動相条件でペプチドをチャージする標準的な HPLC 戦略に戻っています。ペプチドは水への溶解性が限られており(100mg/mLはかなり可溶性が高いと考えられています)、実際の濃度にもかかわらず、大きなサンプル量のカートリッジを装填すると分離能に悪影響を及ぼす可能性があるため、私は溶媒として当初は水を試すのをためらいました。今回では、Octa-Arg は 0.1% 以上の TFA を含む水に容易に溶解し、容易に精製できました(図5)。
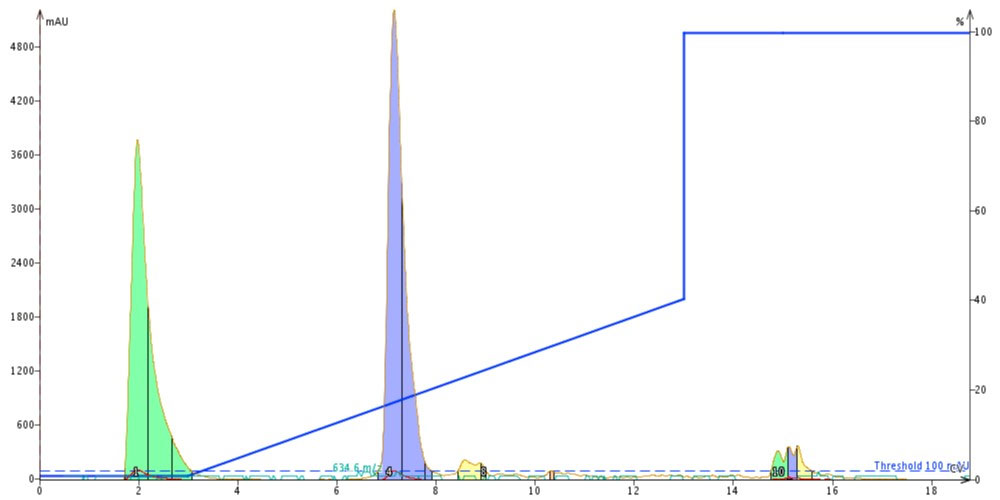
図 5: Oct-Arg を酸性の水に溶解し、精製しました。ペプチド 30mg を 1mL の水に溶解しました。ペプチドは、10CV 以上のアセトニトリル濃度0% ~ 40% のグラジエントで精製しました。
水に TFA を添加することは、精製前のペプチドサンプルを完全に溶解るために重要なポイントとなりました。酸の存在はまた、イオン対形成剤としてのペプチドの全体的な疎水性を増加させるのに役立ち、他の欠損ペプチドなどからのペプチド精製を可能にしました。
親水性ペプチドを精製する際には、チャージする溶媒を慎重に選択しなければなりません。極性溶媒は、典型的には、高濃度のサンプル溶液を作成するには良い選択ですが、移動相と固定相間でのペプチドを分配する移動に影響を及ぼし、精製を妨害することになります。ペプチドを溶解する溶媒を選択する際は、ペプチドサンプルの濃度も重要ですが、ペプチドが保持され、その後容易に精製されるような条件にすることも重要になるかと思います。
親水性の非常に高いペプチドを精製するためには、どのような方法がありますか?
日本語化:2021年12月
ウェブのみ一部修正:2024年8月
PDFファイルダウンロード(2021年12月, 670KB)