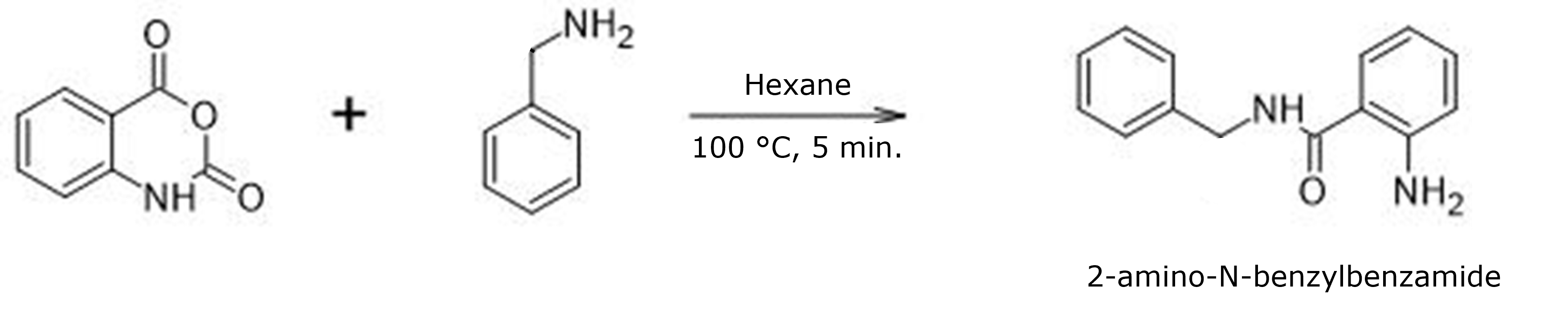
図1:無水イサト酸とベンジルアミンの反応。
この合成について特に難しいことは何もないが、粗生成物の収率と純度は、試薬濃度の違いも含め、上記の各合成項目によって影響を受けると考えられます。試薬の分子量を一定数増やすことで、理論的には化学的相互作用や結合が形成される可能性が高まります。それは事実だが、粗収量と純度が最大になる最適な濃度はあるのだろうか?もしそうなら、それは反応後に生成した反応混合物の精製にどのような影響を与えるのだろうか?
そこで、その答えを明らかにし、その結果を皆さんと分かち合いたいと思い、いくつかの実験を行行いました。私の実験では、試薬の比率はすべて1対2、すなわち1当量の無水イサト酸と2当量のベンジルアミンを使用しました。反応条件は、ヘキサン中で100℃、5分間で、実際の合成はマイクロウェーブ合成装置Biotage® Initiator+で行いました(表1)。
表1:反応スケールの試薬濃度と粗収量。

表1のデータから、実験結果の合成収率が理論収率を上回っていました。これらの差は、副生成物の生成によるもので、もちろん、実際には合成生成物から除去する必要があります。このステップでは、順相フラッシュクロマトグラフィーを用いるのが一般的です。シリカフラッシュカラム(10g、25g、50gのBiotage® Sfär HC)とフラッシュ精製装置Biotage® Selektでヘキサン/酢酸エチルのグラジエントを使用し、多くの極性の低い副生成物や極性の高い副生成物を除去することができました(図2)。
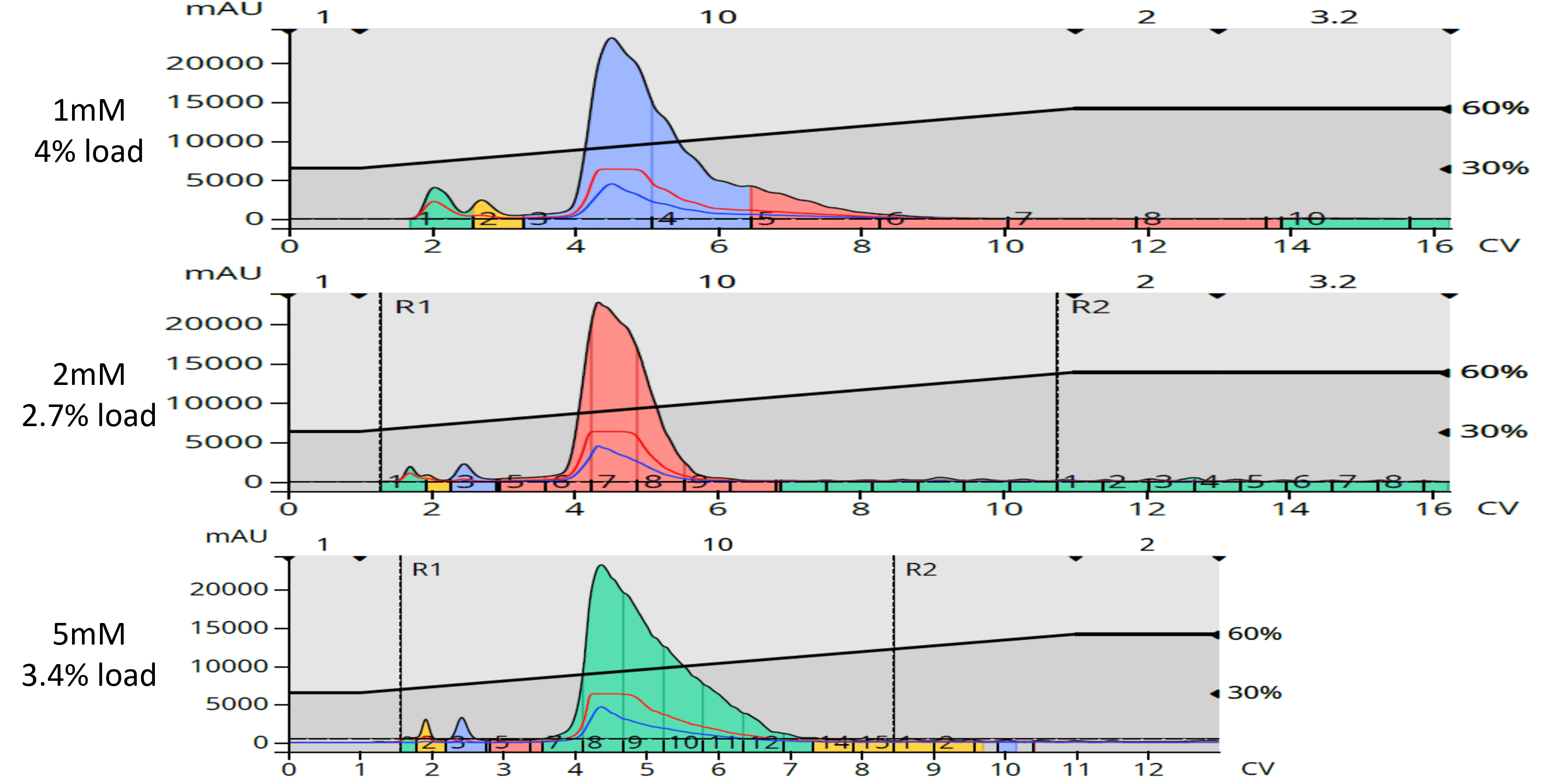
図2:3種類の濃度での反応混合物の順相フラッシュ精製でも同様の結果が得られました。極性の低い副生成物は早く溶出し、極性の高い副生成物は遅く溶出するか、全く溶出しなかった。
予想通り、粗反応混合物の順相でのフラッシュ精製は、主要ピークのフラクションを濃縮した後に回収された化合物の収量を確認すると、最終的な収率は著しく低下しました(表2)。
表2:順相フラッシュクロマトグラフィー生成物収率。

興味深いことに、精製された生成物の収率は1mMの反応で最も低かったが、2mMおよび5mMスケールの反応は非常に近い結果が得られました。しかし、濃縮した精製生成物は、3種類の濃度での反応生成物のそれぞれが、副生成物である無水イサト酸(無水イサト酸は茶色である)の共溶出によるものと思われる茶色/黄褐色を保持していたため、高い純度ではないことがわかりました。
この色を完全に除去するために、順相精鋭で分離した生成物を逆相フラッシュクロマトグラフィー(Biotage® Sfär C18)を用いて水/メタノールのグラジエントで再精製しました。この二次精製(直交精製)は、茶色を除去するだけでなく、これまで知られていなかった、順相精製で生じた副生成物を除去することにも成功しました(図3)。
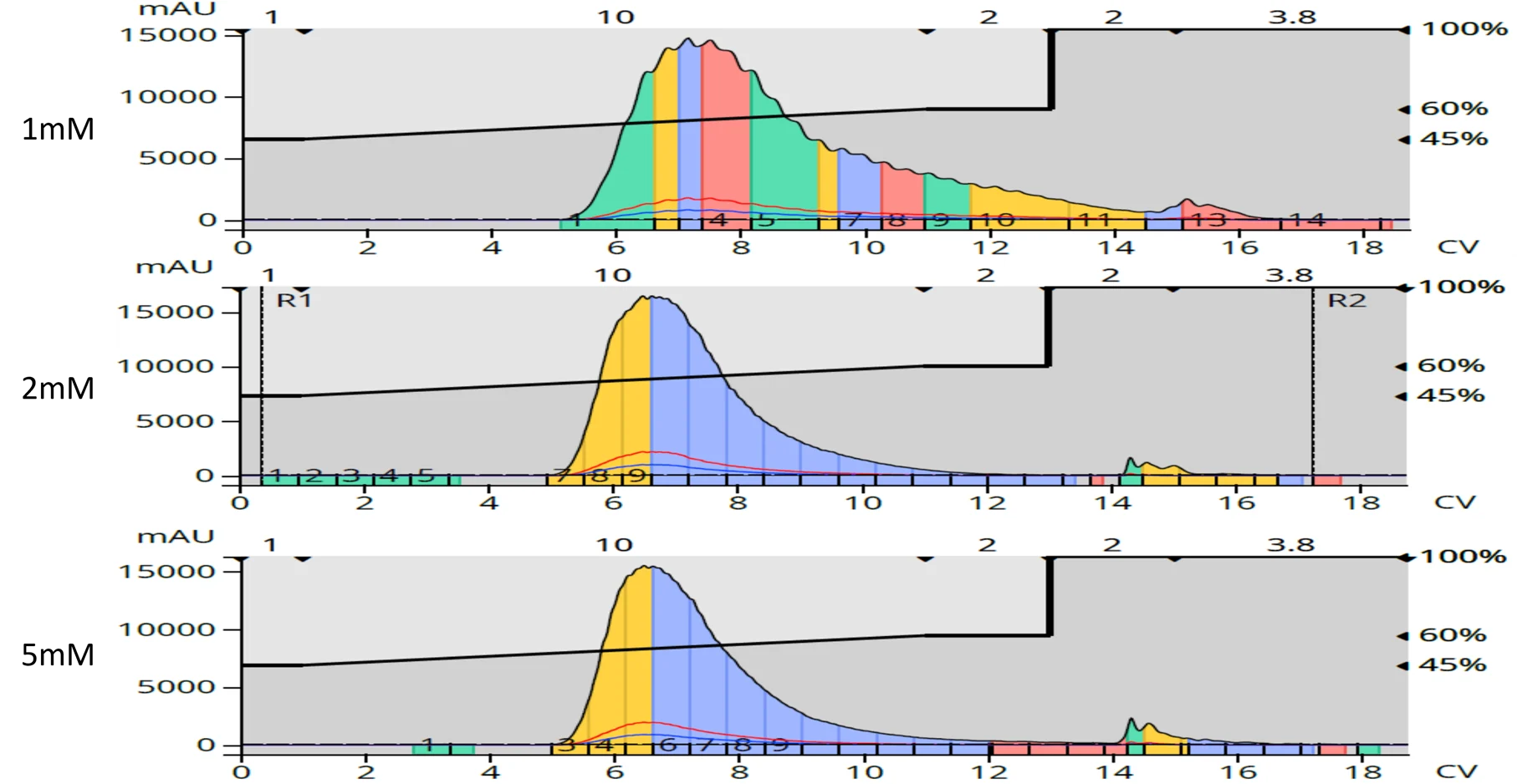
図3:順相精製から単離された生成物の逆相フラッシュ精製により、茶色の原因となる化合物を含む極性および非極性副生成物の両方の化合物が除去されました。
再精製した各生成物ピークを回収し、濃縮させて収率を確認しました(表3)。
表3:逆相フラッシュ精製での生成物の収率。
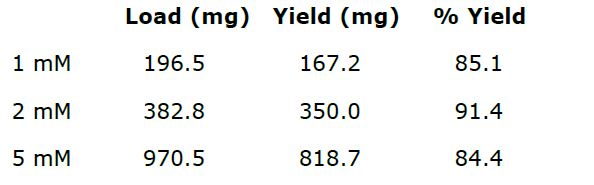
このデータからわかるように、精製後の最大収率は2mMスケールの反応で得られました。このことは、この反応、そしておそらく他の反応においても、収率と純度の両方を最大にする最適な試薬濃度があることを示唆しています。
マイクロウェーブ合成についてもっと知りたい方は、マイクロウェーブ反応チュートリアルをダウンロードして下さい。