October 16, 2020
Bob Bickler
ほとんどのクロマトグラフィー精製では、たった 2つの溶媒で化合物同士を十分に分離することができます。しかし残念ながら、イオン性分子や極性の高い有機分子を含むようなものは、「通常の」溶出条件では分離が不十分であったり、達成できなかったりする場合があります。
この投稿では、この問題に対するいくつかの解決策を提供します。
イオン化可能な化合物は通常、水混和性であり、逆相法 を使用して分離/精製するのが最適です。これらの水溶性化合物の課題は、疎水性(C18)メディアに保持させることと、タイトなバンドで溶出することです。これは、化合物を精製する場合の目標です。これらの両方の目標を確実に達成するには、一般的には pH調整剤または緩衝液(バッファー)が必要です。
なぜか? イオン性およびイオン化可能な化合物は、溶液中で平衡を達成しようと努めているためです(大学時代の pKa、pKb などを覚えていますか?)。これらの化合物は、対イオンが親化合物から部分的に「くっつき」、部分的に「解離」した状態になっています。 これらの分子は異なる平衡状態で存在するため、クロマトグラフィーは困難なものになります。イオン化したものはより極性が高く、早期に溶出する傾向があり、イオン化していないものは保持されます。これにより、テーリングやフロンティングピークが生じます(図1)。
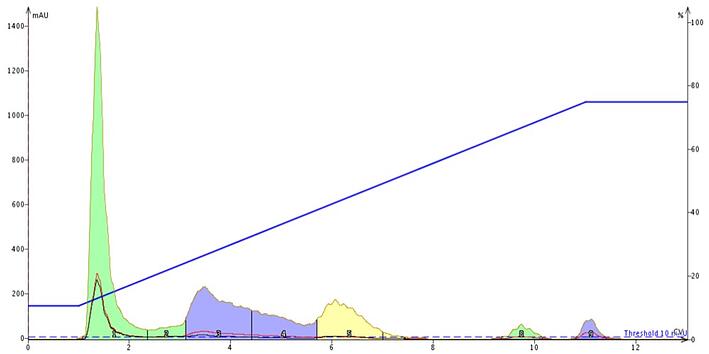
図 1. 水/メタノール勾配を使用したイオン性有機化合物(タートラジン、アルラレッド、ブリリアントブルーFCF、およびエリスロシン(すべての食品着色料))のクロマトグラム。これらの化合物はイオン性が高く解離しやすいため、極性が高く C18 との分配能力を最小にしています。
この問題を解決するには、pHを調整して平衡状態を強制的にどちらかの状態にするか、バッファーを添加してカウンターイオン(対イオン)の会合を強制的に行う必要があります。
酸性および塩基性化合物については、可能であれば 2 pHルールに従うのが好きです。2 pHルールとは、酸をプロトン化するためには、移動相のpHを化合物のpKaより2 pH低くしなければならない、というものです。 同様に、有機アミンを強制的に遊離塩基型にするためには、移動相のpHは化合物のpKaより2 pH高くなければならない。どちらの場合も、化合物が疎水化されることで逆相カラムでの保持力が高まり、通常、ローディング容量とピーク形状の改善(フラクション濃度の増加)により、より良い分離が得られるという利点がある。両方の状況の例を次に示します。
A. 酸性化合物は、移動相が酸性のときに最もよく保持・分離されます。 私は、弱溶出溶媒、強溶出溶媒ともに0.1%レベルの揮発性酸を使用しています。 なぜ揮発性酸なのか?回収容器から化合物を回収する際に、揮発性の酸の方が蒸発させやすいからです。
おすすめの酸は…
i. ギ酸
ii. 酢酸
iii. トリフルオロ酢酸(TFA)
図2は、有機酸(TFA)を添加した逆相クロマトグラフィーにより、3-ニトロ安息香酸(pKa 3.47)、ニコチン酸(pKa 4.85)、ホモバニリン酸(pKa 3.74)という3つの小さな有機酸を保持・分離する方法を示しています。このような低pHの移動相では、これらの酸がプロトン化されて疎水性が高くなり、保持力が高まって分離が向上し、フラッシュ精製を成功させます。
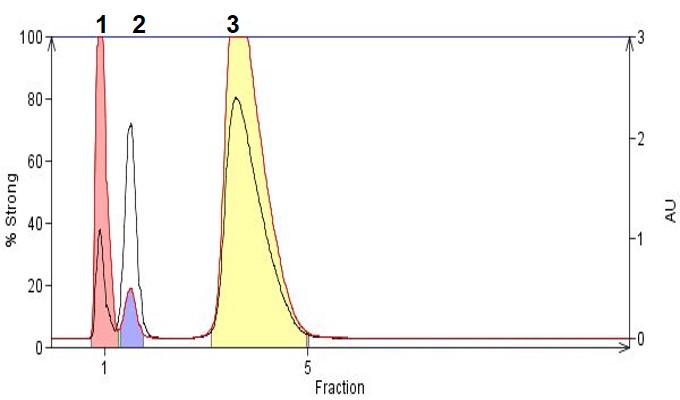
図 2. アセトニトリル/水/TFA(60:40:0.05)の移動相を使用した逆相による有機酸の精製。ピーク1は3-ニトロ安息香酸、ピーク2はニコチン酸、ピーク3はホモバニリン酸です。
B. 同様に、塩基性化合物は、移動相のpHがアルカリ性のときに、最も良好に保持・分離されます。私は弱溶媒と強溶媒の両方で0.1%レベルの揮発性塩基を使用するのが好きです。例えば…
i. 水酸化アンモニウム
ii. ジエチルアミン(DEA)
iii. トリエチルアミン(TEA)
図3に、TEAを塩基として組み込んだグラジエントを使用して、3つの有機アミンである4-ジメチルアミノアンチピリン(pKa 9.6)、N-フェニルベンジルアミン(pKa 3.5)、およびアミトリプチリン(pKa 9.4)を分離した例を示します。上記の有機酸の例と同様に、移動相のpHを化合物のpKaより2単位高い約pH 11に調整すると、疎水性と保持が向上します。これにより、分離が向上し、フラクションの回収が簡単になります(分取したフラクションに含まれる水が少なくなり、有機溶媒が多くなります)。
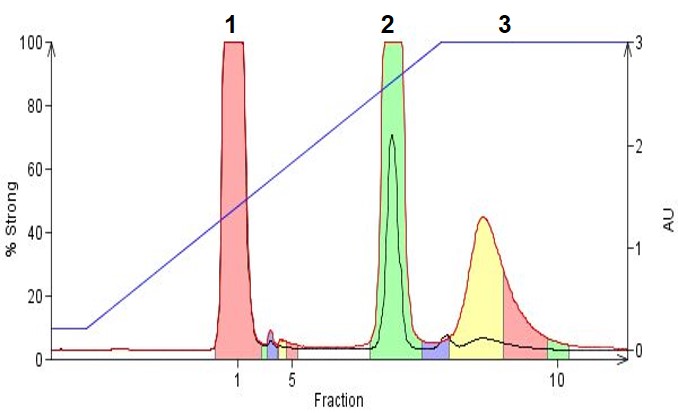
図 3. 逆相グラジエントフラッシュクロマトグラフィーを使用して精製された有機アミン。使用した溶媒は、アセトニトリル、水、0.1%TEA でした。ピーク 1 はジメチルアミノアンチピレン、ピーク 2 は N-フェニルベンジルアミン、ピーク 3はアミトリプチリンです。
荷電性化合物や有機塩の場合は、上記の方法を用いることができますが、化合物が強酸、強塩基、双性イオン である場合(図1の食品着色料の例のように)、揮発性緩衝液(揮発性バッファー)を添加すると分離に驚異的な効果があります。このような場合、私は次の中から選択するのが好きです…
i. ギ酸アンモニウム(10 mM)
ii. 酢酸アンモニウム(10 mM)
食品着色料の例を続けると、揮発性バッファーを添加した場合のクロマトグラフィー分離の改善を図4に示します。この場合のバッファーは酢酸アンモニウム、pH 7でした。揮発性の有機バッファーを添加することで、サンプルの帯電部位はカウンターイオン(対イオン)で「中和」されます。
バッファー濃度はサンプル成分の濃度よりも高いため、サンプルの平衡はこのペアイオンの中和状態に強制され、化合物の親油性が高まり、保持力が高まります。また、イオン部位と対イオンをペアリングすることにより、化学イオン化も最小限に抑えられ、ピーク形状やバンドの広がりに影響を与えることができます(下記参照)。
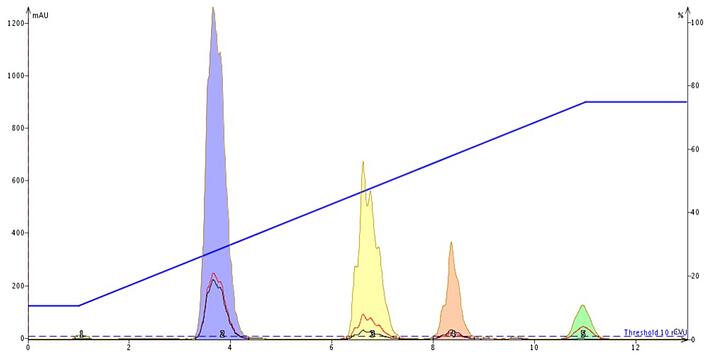
図 4. 酢酸アンモニウムバッファー(pH 7)を溶媒系に加えると、イオン性化合物がより親油性になり、逆相メディアへの保持力が高まります。ピーク形状が改善され、フラクションボリュームが最小限に抑えられます。
移動相にバッファーを加えることにより、そのイオン強度を高めることもできます。イオン を加えることで、移動相の極性が増加します。これは、ウラシルとカフェインを含む DMSO 溶液の精製で見られるように、極性化合物の保持と分離を向上させるのに役立ちます(図5)。移動相のイオン強度を上げ、極性を上げると、ウラシルはC18とよりよく分配され、DMSO から少なくとも部分的に分離されます。カフェインのピーク形状もイオン強度で改善されます。
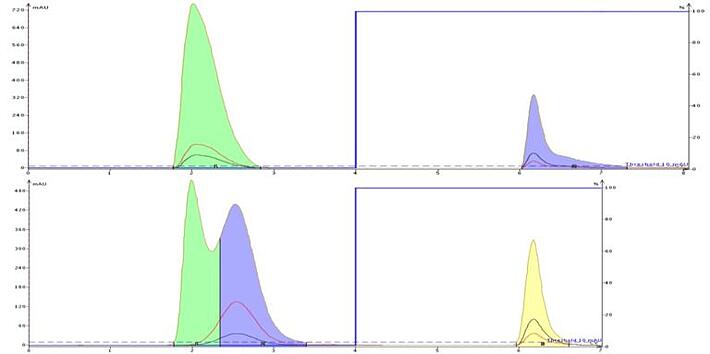
図 5. 非イオン性化合物には、溶媒をより極性にするバッファーが有効です。上のクロマトグラムでは、ウラシルは注入溶媒であるDMSOと共溶出し、カフェインは保持されていますが、若干のテーリングが見られます。バッファーを添加すると、ウラシルの保持が改善され、カフェインがよりタイトなバンドで溶出します。
したがって、サンプルのイオン性またはイオン化可能な化学的性質に最適な精製方法を構築するには、適切な溶媒条件(酸、塩基、またはバッファーを追加)を選択して、フラクションボリュームを最小にしながら分離効率と負荷量を最大にすることが必要です。
このような困難な精製にどのように取り組んできましたか?
フラッシュメソッドの開発と最適化の詳細については、下記ボタンからホワイトペーパーをご覧ください。
日本語化:2022年2月
ウェブのみ一部修正:2024年9月
PDFファイルダウンロード(810KB, 2022年2月)