August 12, 2020
Bob Bickler
合成化学者は、新規の化合物を作る方法を常に模索しています 。その過程で、試薬、溶媒、反応条件などを検討し、さまざまな反応生成物や副生成物が生じます 。
反応生成物の精製には、多くの場合、フラッシュクロマトグラフィーが使用され、分析、化合物の同定、合成収率の決定などが行われます。合成がうまくいけば高純度の生成物が得られることもありますが、逆に多くの化合物が混ざって精製が困難になることもあります。
有機化学の反応は、どんなに単純なものでも、複雑な混合物になることがあります。私が最近遭遇したのは、有機酸(ニコチン酸)と有機塩基(ベンジルアミン)を反応させてアミドを生成するという、一見単純な反応でした(図 1)
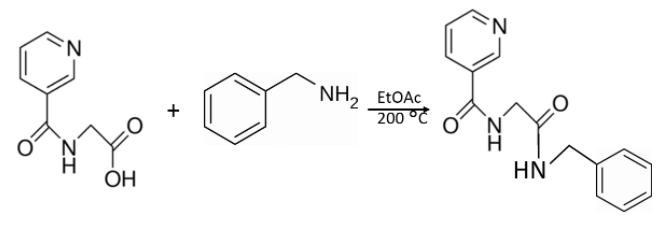
図 1. ニコチン酸とベジルアミを 200℃の酢酸エチル中で 10分間反応させると、図のようなアミドが生成されます。
ニコチン酸の溶解度は低いですが、反応溶媒として酢酸エチルを使用しました。ただし、200°Cで反応させると、ニコチン酸は可溶化してベンジルアミンと反応します。
合成後、冷却すると結晶ができました。結晶をろ過し,酢酸エチルで洗浄した後, フラッシュマスシステムの Biotage® Isolera Dalton 2000で分析したところ,生成物( M+H 270)と過剰なニコチン尿酸(M+H 181)の両方が含まれており,結晶の総質量は 43mgでした。
母液(明るい黄色)を様々なヘキサン/酢酸エチル比でTLC分析し ましたが、目的物はベースラインからほとんど動かなかったため、精製には逆相を使用することにしました( 10CVで 25-75%のメタノールリニアグラジエント)。12gの Biotage® Sfär C18 カラムと高速自動フラッシュ精製システム Biotage® Selekt を使用しました。化合物は保持されましたが、分離は理想的とは言えません(図 2)。
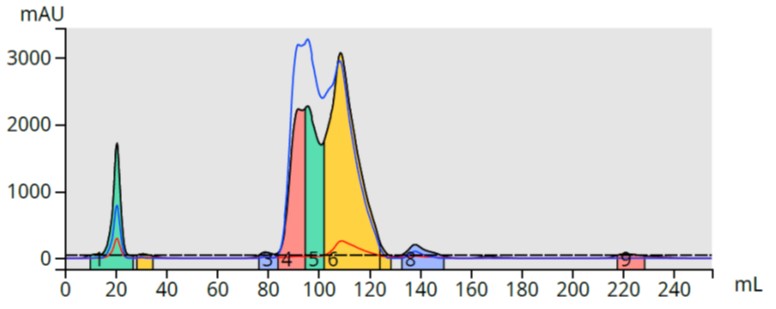
図 2. 反応混合物の逆相フラッシュ精製 。生成物 (黄色)は主要な副生成物から部分的にし離されていません 。
グラジエント条件の最適化 やさまざまな溶媒の検討に時間をかけるよりも、ドライローディングに イオン交換 メディア ( ISOLUTE® SCX-2 )を 試すことにしました。なぜ SCXなのか? アミド生成物は理論的には中性で電荷を帯びていませんが、新たに追加されたアミン官能基は、アニオン性官能基(プロピルスルホン酸)に引き付けられるはずです。もしそうであれば、母液を SCXメディアと混合して乾燥させることで、「新しい」アミドの窒素(ベンジルアミン反応による)と SCXのスルホン酸が強制的に反応し、後で塩基性溶媒でリリースできるように生成物をトラップすることができるはずです。もしこれがうまくいけば、私の生成物は SCXに吸着し、不純物は吸着しないはずです。
最初にスモールスケールで実験を行ったところ、図 3に示すように、1%のNH4OH を含むメタノールで目的物が溶出し、この理論が成り立つことがわかりました。

図 3. 強陽イオン交換媒体( SCX )を使った反応混合物の逆相フラッシュ精製。
しかし、フラクション14(図 3のピンクのピーク)を分析したところ、目的の化合物だけでなく、その他の副生成物も結合/放出されていました。主要な不純物が除去されているので問題はなく、元の 25-75%のメタノールグラジエントを用いて再精製すれば、他の副生成物と目的物が分離されるはずです 。
生成物のフラクション #14 を C18 の Samplet® カートリッジ のメディア上で乾燥させ、元の方法で再精製したところ、 目的物と塩基性副生成物が完全に分離されました(図 4)。

図 4. SCX で再精製したフラクションは、初期に溶出不純物がすべて除去されてい ます 。
この成功を受けて、残りの母液(約 1g)を 5gの SCXメディアと 前と同じC18カラムを用いて精製しました。この負荷は12gの C18カラムでは過剰ですが、 SCXメディアを使用して 目的物 を「 補足 」して濃縮し、主要な不純物がかなり早い段階で溶出したため、負荷を最大にすることができたと考えています。
クロマトグラフィーは厄介ですが、最終的には成功した精製を示し、主要な副産物の汚染物質が早期に溶出し、私の生成物はフラクション15〜17に塩基での洗浄で溶出しました(図 5)。

図 5. 5g の ISOLUTE SCX-2 を用いて反応混合物ラージスケルでフラッシュ精製 。SCX-2 は生成物(大きなピンクのピーク)を捕捉します 。
フラクション15-17 を乾燥させると、330mg の黄色の固体が得られ、これを再精製すると、 目的物フラクション(フラクション5-7)が無色の、 よりきれいな目的物のクロマトグラムが得られました(図6)。

図6. SCXで再精製したフラクションでは、主要な反応副生成物が完全に除去されているが、他の副生成物がいくつか存在していました。目的の反応生成物はピンク色のピークで、回収容器では無色でした。
フラクション 6 を蒸発させると、200 mg の純粋な生成物が得られました(図 7)。

図7. 図 6 のフラクション 6 からの乾燥した反応生成物。
複雑で精製が困難な反応混合物の精製は、機能化されたドライロードメディアを使用することで改善できることが よくあります 。 以前 、同じ SCXメディアを使って、反応混合物から アミンの副生成物をスカベンジ(除去)する方法 をご紹介しました。
フラッシュクロマトグラフィーの詳細については、下記ボタンからホワイトペーパーをご覧ください。
日本語化:2021年7月
ウェブのみ一部修正:2024年9月
PDFファイルダウンロード(856KB, 2021年7月)