April 13, 2020
Bob Bickler
一般的なリニアグラジェントやTLCベースのグラジエントを使用している多くの化学者にとって、精製結果は混合物中のすべての化合物を分離するのに十分な選択性を持っていないことがよくあります。 これは、ターゲットに溶出しやすい不純物がある場合に特に当てはまります。分離能を高めるために用いられる方法の1つに、精製中にアイソクラティックホールドやグラジエントポーズを用いる方法があります。
この記事では、アイソクラティックホールドがどの程度有効なのか、またグラジエントメソッドにいつ/どのように挿入したらよいのかを検討します。
クロマトグラファーとしてのキャリアにおいて、私は多くの賢人に会いました。彼らは、クロマトグラフィーを観察し、化合物が溶出し始めたらグラジエントを一時停止するかアイソクラティックホールドを挿入すれば、その溶出化合物の分離が改善されると断言します。私には、これは非論理的に思えます。
なぜなら、ピークが検出された時点で、その化合物はすでにカラムから出ているからです(図1)。 固定相とカラム内の溶媒との相互作用によって、すでに分離が行われているのです。 この時点でアイソクラティックホールドを挿入しても、遅すぎます。まだカラムに入っていない溶媒ブレンドにしか影響を与えないからです。後から溶出する化合物にしか影響が現れないのです。これについてさらに考えてみると、アイソクラティックホールドの影響が出る前に、少なくとも1本のカラム容量分のアイソクラティック溶媒ブレンドが必要であることは論理的に予測できるのではないでしょうか?
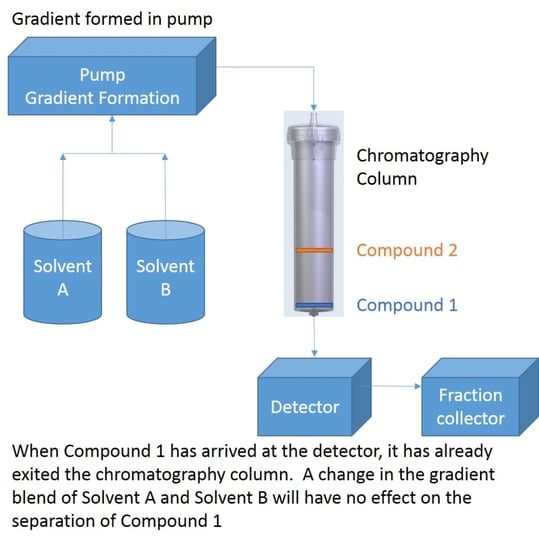
図1. 2つの化合物の溶出を示すフラッシュクロマトグラフィーシステムの配管図。化合物1はカートリッジを出て検出器に入るので、グラジエントを変更しても隣接する化合物との分離に影響を与えません。
以前の投稿で、フラッシュ精製を最適化する方法、特にTLCを利用する方法について述べました。アイソクラティックホールドについて、分離にホールドを適用することが適切かどうか、またいつ適用するのが適切かを調べるために、最近実験してみたものです。
TLC
まず、5成分混合物を 20% 酢酸エチル/80% ヘキサンで TLC を行い、Rf 値を計算し、それを使ってリニアグラジエントを構築しました。
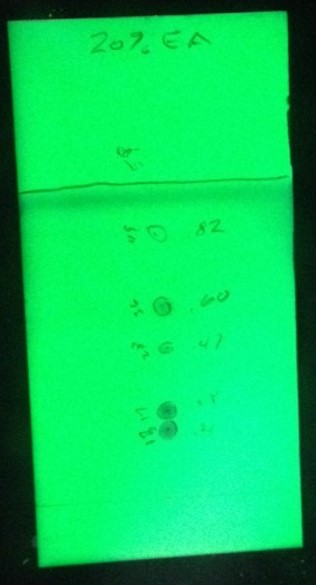
図2. 20%EtOAc での TLC 分離では、下の 2 つのスポットが典型的な8の字型に分離していることがわかります。これほど近くで溶出する化合物は、フラッシュクロマトグラフィーで分離することが難しい場合があります。
TLC の結果、下の 2 つの化合物は古典的な 8 の字パターンで互いに密接して溶出することがわかり、分離がやや難しく、ローディング容量は最小になります(表1)。
表1. RfとCVの計算
| Rf | CV | |
|---|---|---|
| Compound 1 | 0.82 | 1.22 |
| Compound 2 | 0.6 | 1.67 |
| Compound 3 | 0.47 | 2.12 |
| Compound 4 | 0.29 | 3.45 |
| Compound 5 | 0.22 | 4.54 |
フラッシュシステムの TLC からグラジエント機能を用いて、上記の TLC から 5% から 40% の EtOAc のリニアグラジエントからなるメソッドを作成しました。 ロード量は 100 mg、カラムは Biotage® ZIP 10 g シリカカラムを使用しました。
Flash chromatography (フラッシュクロマトグラフィー)
リニアグラジエントにより、すべての化合物が分離されましたが、最後の2つは完全に分離されませんでした(図3)。
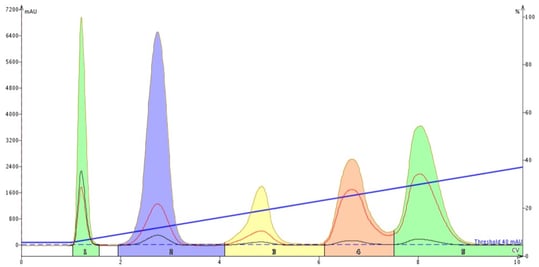
図3. TLC ベースのリニアグラジエントにより 5 つの化合物すべてが分離されましたが、最後の 2 つは完全に分離されていません。
次に、同じグラジエントを再実行しましたが、化合物4(ピンク色のピーク)が溶出し始めると同時に、アイソクラティックホールドを挿入しました。その場でのアイソクラティックホールドでは、分離は改善されませんでした(図4)。
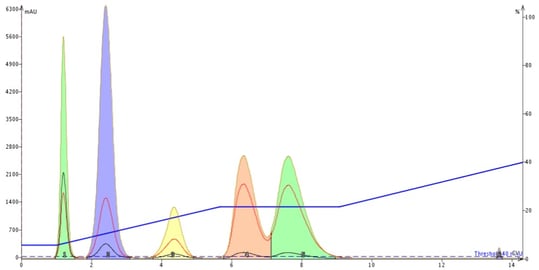
図4. ピーク 4 のスタートに on the fly でアイソクラティックホールドを挿入しても、元のリニアグラジエントと比較して、ピーク 4 とピーク 5 間の分離度は変わりませんでした。
上記のロジックに基づき、私はグラジエントを編集し、化合物4の溶出前に 1CV(カラム容量)のアイソクラティックホールドを組み込みました。つまり、5CV でホールドが始まるように設定しました。これを効果的に行うには、最初のグラジエントの勾配を維持する必要があり、3.5%/CV の場合、5 CV でグラジエント中の % EtOAc は 19%(3.5%/CV×4 CV = 14%、14% + 最初の 1 CV グラジエントの開始 5% = 19%)となりました。ピーク 5 が完全に溶出した後に終了するように、ホールドの長さを 4CV に設定しました。 その結果、この修正したメソッドは、その場でのホールド挿入とほぼ同じパフォーマンスであることがわかりました(図5)。
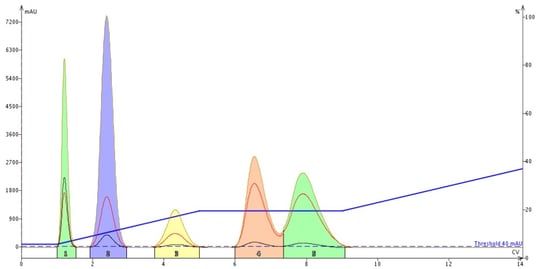
図5. 化合物 4 の溶出前にアイソクラティックホールド 1CV を構築した結果、化合物 5 との分離にほとんど影響はありませんでした。
そこで、もう少し考えて、アイソクラティックホールドの開始点を 3CV に下げました。なぜ、3CV にしたのか? それは、基本的に直感です。 この新しい開始点に基づいて、グラジエントの EtOAc ターゲットを 12% に設定しましたが、新しいホールド開始点による 2CV の追加を補うためにホールドボリュームを 6CV に増やしました。
さて、このメソッドを実行したところ、なんと、図6 のように、確かに化合物 4 と 5 の分離が改善されたのです。 その理由は、新しい溶媒条件での平衡化の再開と関係があるのではないかと考えています。
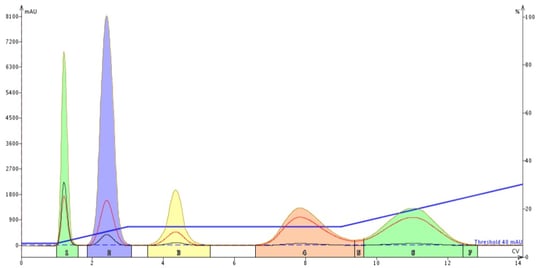
図6. 溶出前に 4CV のアイソクラティックホールドをプログラムすることで、ピーク 4 と 5 の間がほぼベースラインまで分離が改善されました。
ドライフラッシュカートリッジは通常、最低 3CV で平衡化されます。このデータは、リニアグラジエントにアイソクラティックホールドをプログラムする際の最低必要量であることを示唆しています。この理論に基づくと、私の提案は、低い分離度の化合物のペアのうち先に溶出が始まると予想される 3CV 前に、アイソクラティックホールドを挿入することです。
では、精製を行ったことがなく、TLC のデータしかない場合、グラジエント中にホールドを挿入すべき時点をどのように推定すればよいのでしょうか?
その答えは、TLC データの中にあると思います。 上記の表1 では、化合物 4 の Rf は 0.29(スポットの中心)であり、CV は 3.45 に相当します。 これは、20% 酢酸エチルで精製した場合、化合物 4 はその頂点が約 3.45 CV で溶出することを意味します。 化合物は常にバンドで溶出し、ガウス分布でグラフ化されるので、検出は早くから行われます。
グラジエントで溶出することにより、各化合物の溶出量が遅れるので、必要に応じてどこかにアイソクラティックホールドを挿入する自由を与えます。 私の理論では、TLC データから計算した CV を2倍すると、その化合物の頂点が TLC ベースのグラジエントで溶出するのに必要な CV の数を概算できるというものです。 その数値が決まったら、その化合物の予測される溶出 CV(頂点)の 4CV 前にアイソクラティックホールドを設定します。 4CV 前に設定することで、ピークのリーディングエッジが補正され、カートリッジが再平衡化されることを確認します。
アイソクラティックホールドの開始点を決定するのに役立つ方程式は以下のとおりです。
CV = 1/Rf
Hold start (CV) = (CV*2) – 4
私のサンプルでは,化合物 4 の TLC Rf 値が 0.29 であることから、CV は 3.45 となります。 これを 2 倍にすると、6.9 CV という値になります(フルリニアグラジェントでのピーク頂点での実際の溶出量は 6.7 CV でした)。 ピークの始まりに 1CV を考慮し、3CV でアイソクラティックホールドを開始すると、カートリッジがアイソクラティック混合溶媒中で再平衡化するのに十分な時間が得られ、分離にプラスの影響を与えることがわかりました。
上記の私のサンプルでは…
CV = 1/Rf = 1/0.29 = 3.45
Hold start = (CV*2) – 4 = (3.45*2) – 4 = 2.9 CV
つまり、この計算では、プログラムされたグラジエント法で、2.9(または3)CV でアイソクラティックホールドを挿入することになります。
困難な分離を改善するためにグラジエントホールドを挿入したことがありますか? その場合は、その経験を私たちと共有してください。
フラッシュクロマトグラフィーについてもっと知りたいですか?フラッシュクロマトグラフィーの詳細については、ホワイトペーパーをご覧ください。
日本語化:2022年11月
ウェブのみ一部修正:2024年9月
PDFファイルダウンロード(1MB, 2022年11月)